

热点新闻
- 利德曼闪耀CACLP 2025:创新
- 邀请函丨利德曼邀您共聚
- 利德曼获评中上协“2024上
- 利德曼再次入选 “北京专
- 利德曼与苏州立禾生物正
- 利德曼荣获“证券之星·资
- 利德曼与俄罗斯VT公司达成
- 利德曼荣获《中国基金报
- 清远市市委副书记、市长
- 中国品牌日丨 利德曼以品
- 活动回顾丨响应健康中国
- IFCC执行委员会秘书长及北
- 公司动态丨利德曼2023年度
- 2024年会盛典丨利德曼年会
- 喜报|利德曼获评北京经开
- 科研创新│利德曼ST2科研
- 科研创新 │ 利德曼子公司
- 喜讯丨利德曼荣登2023北京
- 会议回顾丨第二届ZAODX世界
- 会议预告丨利德曼与您相
- 汇聚智慧 :善济学社第一
- 热烈祝贺:广开控股生命
- 广州开发区管委会副主任
- 广州市黄埔区委书记陈杰
- 利德曼与高博医疗集团达
- 喜讯!利德曼成功入选“
- 喜讯!利德曼获评北京市
- 喜讯!利德曼医学参考实
- 利德曼荣获经开区五星公
- 利德曼签约MAI47、纷享销客
- 利德曼与润达医疗达成战
- 利德曼董事长王凯翔先生
- 喜讯!利德曼医学参考实
- 阿匹斯科技两项新型冠状
- 心系武汉|北京利德曼向湖
- 喜讯:利德曼荣获“科技
- “乘风.破浪.共创.辉煌”
- 喜讯:利德曼喜迎高新科
- 感恩有你 一路同行 丨利德
- 强强联手 共铸辉煌 | 利德
- 喜讯:利德曼荣获“2018年
- 喜讯:利德曼参考实验室
- 利德曼成功举办2018年代理
- 利德曼盛大亮相2018美国芝
- 利德曼在2017年RELA试验中再
- 利德曼在2018年卫生部参考
- 为促进医学装备领域发展
- 山水之都,美丽重庆!利
- 利德曼荣获“2017年度中国
- 2017全国检验大会圆满落幕
喜讯!利德曼医学参考实验室顺利通过CNAS扩项评审
作者:利德曼日期:2022-05-24
近日,经中国合格评定国家认可委员会(以下简称“CNAS”)批准,北京利德曼生化股份有限公司医学参考实验室申请的5个参考测量能力项目扩项评审顺利通过。本次通过的项目包括葡萄糖(GLU)、尿素(UREA)、尿酸(UA)、总胆红素(TBIL)、总蛋白(TP),涉及“代谢物和底物”、“蛋白质”两个领域。其中,尿酸(UA)项目为分光光度法原理的参考测量方法,该方法为国内率先获得CNAS认可的实验室。我司医学参考实验室对上述5个项目的参考测量能力和水平已符合国际标准,为公司高质量产品提供了保障。(相关信息可见网址:https://las.cnas.org.cn/LAS_FQ/publish/externalQueryL1.jsp)
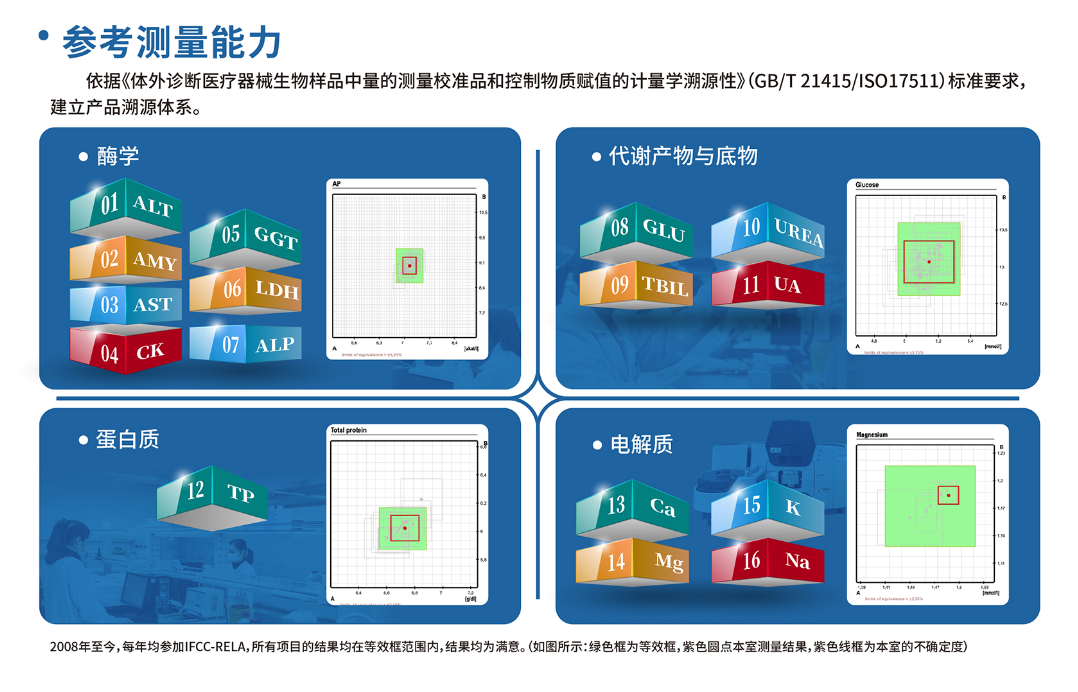
我司医学参考实验室获CNAS认可的项目达12项,分别是:
• 代谢物和底物:GLU、UREA、UA、TBIL
• 蛋白质 :TP
• 酶:ALT、AST、GGT、CK、LDH、AMY、ALP
CNAS是中国唯一加入国际认可论坛(IAF)、国际实验室认可合作组织(ILAC)、亚太实验室认可合作组织(APLAC)和太平洋认可合作组织(PAC)的代表机构,在国内和国际上被视为是实验室技术能力和管理能力的可靠性依据,通过认可的实验室出具的检测/校准报告具有CNAS和ILAC的标识。


利德曼医学参考实验室
利德曼医学参考实验室致力于公司产品溯源体系的建立和维护,主要承担建立量值溯源及参考方法,参加国内外权威机构组织的能力验证,完成企业校准品的研制、赋值、监测及管理的相关工作,为公司产品质量保驾护航。发展历程:2006年,正式组建2008年,首次通过IFCC-RELA酶学项目2009年,首次通过IFCC-RELA代谢产物与底物项目2010年,首次通过IFCC-RELA蛋白质项目2011年,首次通过IFCC-RELA离子类项目(我国首家将原子吸收平台应用于离子参考测量的实验室);起草行业标准YY/T 1195-2011《血清总蛋白参考测量程序》(我国首个生化诊断领域参考方法行业标准)2014年,依据ISO/IEC ISO17025和ISO15195建立实验室质量管理体系2015年,完成北京市专项课题《医疗器械(体外诊断试剂)检测与参考品评价服务平台》(与中国食品药品检定研究院合作)2018年,获得CNAS认可2019年,完成北京市科技计划课题《G20工程龙头企业培育——生化诊断试剂质量性能评价研究及标准品体系建立》(与卫生部临检中心、北京市医疗器械检验所等单位合作)2021年,进入JCTLM参考测量服务实验室数据库2022年,CNAS扩项评审通过,我司医学参考实验室获CNAS认可的项目共计12项
继往开来,砥砺前行,利德曼也将秉承“深耕专业诊断,提供信赖服务,以生命科学改善人类生活”的使命,依据CNAS认可的检测流程及标准,以产品质量为企业核心生命力,持续提升品牌竞争力!








